Arten der Enzymhemmung



Kleiner Tipp:
Wenn du die Seite neu lädst, sind alle Bestandteile wieder "aufgeräumt";)
Fertige mit Hilfe der vorgegbenen Objekte eine modellhafte Darstellung einer Art der Enzymhemmung (kompetitiv oder allosterisch) an. Mache einen Screenschot deiner Darstellungen. Du kannst hier zusätzliche Beschriftungen einfügen, oder du beschriftest deine Darstellung auf dem Screenshot. Lade diesen Screenshots bei Moodle hoch.


Enzyme sind Biokatalysatoren, die chemische Reaktionen in lebenden Organismen beschleunigen, indem sie die Aktivierungsenergie herabsetzen. Ihre Aktivität kann jedoch durch spezifische Moleküle, sogenannte Inhibitoren, gehemmt werden. Dabei wird zwischen irreversibler und reversibler Hemmung unterschieden, wobei beide Mechanismen unterschiedliche Auswirkungen auf das Enzym und dessen Funktion haben.
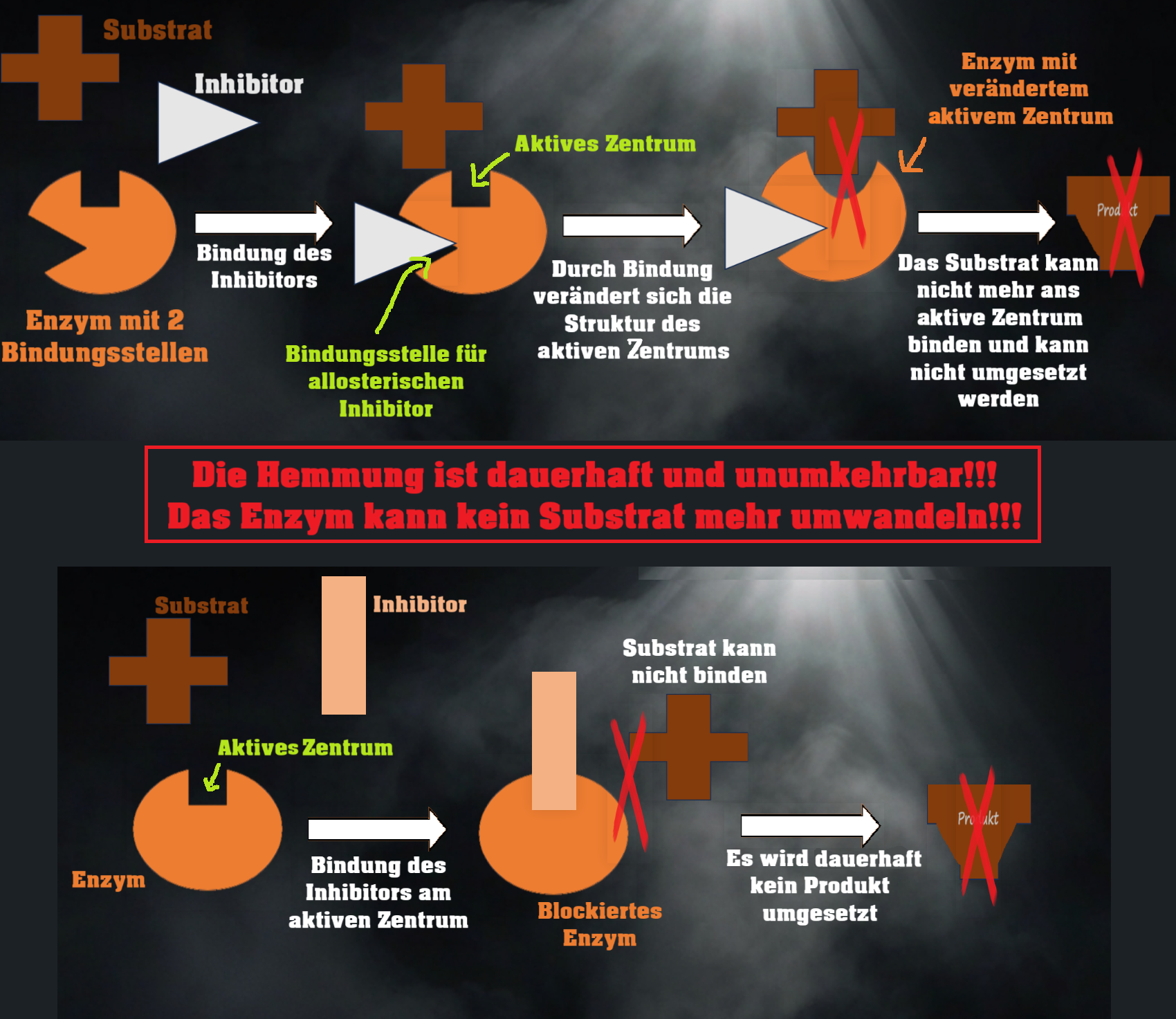
"Bei der irreversiblen Hemmung bindet der Inhibitor dauerhaft(!) an das Enzym, wodurch dessen katalytische Aktivität unumkehrbar verloren geht. Dies kann auf zwei Arten geschehen:
1. Ein Inhibitor kann direkt mit dem Substrat um das aktive Zentrum konkurrieren, daran binden und es so dauerhaft blockieren.
2. Alternativ kann ein Inhibitor an einer anderen Stelle des Enzyms binden, was eine strukturelle Veränderung des aktiven Zentrums verursachen kann, sodass das Substrat nicht mehr an das aktive Zentrum andocken kann.
In beiden Fällen wird die enzymatische Reaktion verhindert, und das gewünschte Produkt kann nicht mehr gebildet werden. Besonders toxische Substanzen wie Schwermetalle oder Nervengifte nutzen diesen Mechanismus."
Enzyme sind Biokatalysatoren, die chemische Reaktionen in lebenden Organismen beschleunigen, indem sie die Aktivierungsenergie herabsetzen. Ihre Aktivität kann jedoch durch spezifische Moleküle, sogenannte Inhibitoren, gehemmt werden. Dabei wird zwischen irreversibler und reversibler Hemmung unterschieden, wobei beide Mechanismen unterschiedliche Auswirkungen auf das Enzym und dessen Funktion haben.
Im Gegensatz zur irreversiblen Hemmung ist die reversible Hemmung nicht dauerhaft, da der Inhibitor nur vorübergehend an das Enzym bindet. Die Hemmwirkung kann durch veränderte Bedingungen, wie eine Erhöhung der Substratkonzentration oder die Entfernung des Inhibitors, rückgängig gemacht werden.
Es gibt zwei Hauptformen der reversiblen Hemmung:
- Kompetitive Hemmung
- allosterische Regulation"
Enzyme sind Biokatalysatoren, die chemische Reaktionen in lebenden Organismen beschleunigen, indem sie die Aktivierungsenergie herabsetzen. Ihre Aktivität kann jedoch durch spezifische Moleküle, sogenannte Inhibitoren, gehemmt werden. Dabei wird zwischen irreversibler und reversibler Hemmung unterschieden, wobei beide Mechanismen unterschiedliche Auswirkungen auf das Enzym und dessen Funktion haben.
Die kompetitive Hemmung ist eine Form der Enzymhemmung, bei der der Inhibitor eine dem Substrat ähnliche Struktur besitzt. Dadurch konkurriert er mit dem Substrat um das aktive Zentrum des Enzyms. Solange der Inhibitor dort gebunden ist, bleibt das aktive Zentrum blockiert, und das Substrat kann nicht umgesetzt werden.
Enzyme sind Biokatalysatoren, die chemische Reaktionen in lebenden Organismen beschleunigen, indem sie die Aktivierungsenergie herabsetzen. Ihre Aktivität kann jedoch durch spezifische Moleküle, sogenannte Inhibitoren, gehemmt werden. Dabei wird zwischen irreversibler und reversibler Hemmung unterschieden, wobei beide Mechanismen unterschiedliche Auswirkungen auf das Enzym und dessen Funktion haben.
Bei der allosterischen Regulation bindet der Inhibitor nicht an das aktive Zentrum, sondern an eine allosterische Bindungsstelle des Enzyms. Diese Bindung verändert die räumliche Struktur des Enzyms, sodass entweder das aktive Zentrum selbst verändert wird oder dessen Affinität zum Substrat abnimmt.

Als Beispiel ist hier ein Modell einer normalen enzymatisch katalysierten Reaktion zu sehen. Nach diesem Prinzip kannst du versuchen, ähnliche Modelle zu den unterschiedlichen Arten der Hemmung zu erstellen.
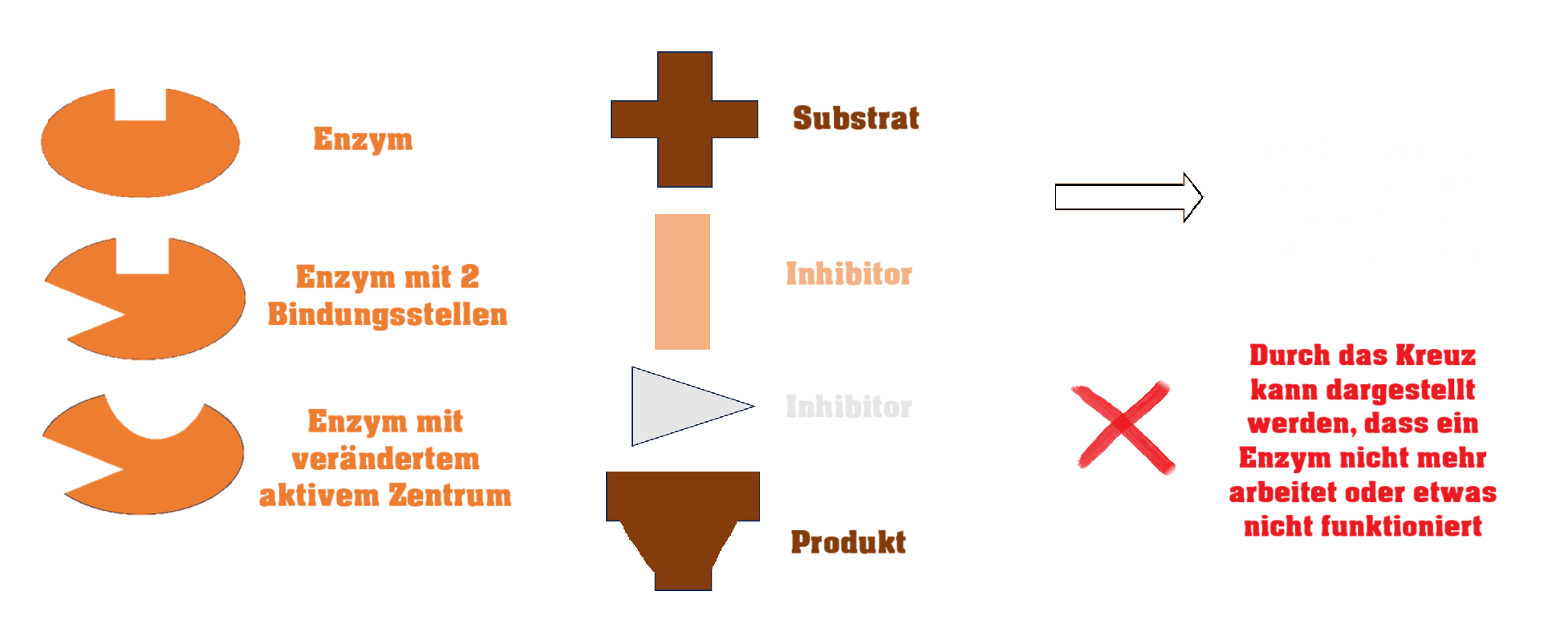

1. Versucht, nach dem Lesen des Infotextes, die Art der Hemmung zuerst zu erklären.
2. Überlegt, welche Formen (Bestandteile) ihr benötigt, um die entsprechende Hemmung darstellen zu können. (Benötigt ihr alle Formen oder nur bestimmte?)
3. Überlegt, was der Ausgangszustand ist.
4. Überlegt, was in welcher Reihenfolge passieren muss.
5. Wenn es mehrere Möglichkeiten gibt, könnt ihr auch zwei Modelle untereinander anfertigen.
Schreibe in das Textfeld unten und ziehe es an dem grauen Rand an die richtige Stelle.
1. Überlege, ob die Form des Produkts sinnvoll gewählt wurde.
Begründe deine Antwort
– warum passt sie oder warum nicht?
2. Überlegt, ob es Szenarien gibt, die eine Enzymhemmung sinnvoll machen.




Wähle ein Beispiel aus und entscheide, um welche Art der Hemmung es sich handelt.
Richtig = Punkt
Falsch = Minuspunkt
Viel Spaß!

Bei der irreversiblen Hemmung bindet der Inhibitor dauerhaft an das Enzym, wodurch dessen katalytische Aktivität dauerhaft verloren geht. Dies geschieht oft durch kovalente Modifikationen am aktiven Zentrum oder an anderen funktionellen Bereichen des Enzyms. Besonders toxische Substanzen wie Schwermetalle oder Nervengifte nutzen diesen Mechanismus.
Reversibel bedeutet, dass diese Form der Hemmung wieder rückgängig gemacht werden kann!
Die kompetitive Hemmung ist eine Form der Enzymhemmung, bei der der Inhibitor eine dem Substrat ähnliche Struktur besitzt. Dadurch konkurriert er mit dem Substrat um das aktive Zentrum des Enzyms. Solange der Inhibitor dort gebunden ist, bleibt das aktive Zentrum blockiert, und das Substrat kann nicht umgesetzt werden.
Bei der allosterischen Regulation bindet der Inhibitor nicht an das aktive Zentrum, sondern an eine allosterische Bindungsstelle des Enzyms. Diese Bindung verändert die räumliche Struktur des Enzyms, sodass entweder das aktive Zentrum selbst verändert wird oder dessen Affinität zum Substrat abnimmt.













































